WikiZero - Етан
open wikipedia design.
Етан 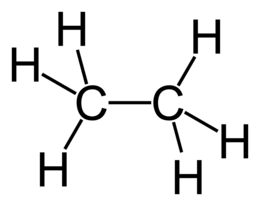
 загальні систематичне
загальні систематичне
найменування Етан Хім. формула C2H6 Рац. формула H3CCH3 Фізичні властивості стан газ молярна маса 30,07 г / моль щільність 1,2601 кг / м³ в стандартних умовах по ГОСТ 2939-63; при н. у. (0С) 0,001342 г / см Термічні властивості Т. плав. -182,8 ° C Т. кип. -88,6 ° C Т. доп. 152 ° C Т. воспл. 152 ° C Т. свспл. 472 ° C Мовляв. теплоємність. 52,65 Дж / (моль · К) ентальпія освіти -84,67 кДж / моль Тиск пара 2,379 МПа (0 ° С) Хімічні властивості pKa 42 (вода, 20 ° С) Класифікація Реєстр. номер CAS 74-84-0 PubChem 6324 Реєстр. номер EINECS 200-814-8 SMILES InChI RTECS KH3800000 ChEBI 42266 і 42260 номер ООН 1035 ChemSpider 6084 Безпека токсичність Малотоксичний. Володіє слабким наркотичною дією H-фрази
H220, H280
[1] P-фрази P210, P377, P381, P410 + P403 сигнальне слово небезпечно піктограми СГС 
 Наводяться дані для стандартних умов (25 ° C, 100 кПа) , Якщо не вказано іншого.
Наводяться дані для стандартних умов (25 ° C, 100 кПа) , Якщо не вказано іншого.
Етан ( лат. ethanum), C 2 H 6 - органічна сполука, другий член гомологічного ряду алканів . Газ без кольору і запаху. У промисловості етан отримують з природного газу і нафти і витрачають переважно для виробництва етилену .
Етан при н. у. - безбарвний газ , Без запаху і смаку. Молярна маса - 30,07. Температура плавлення -183,23 ° C, Температура кипіння -88,63 ° C. Щільність ρгаз. = 0,001342 г / см³ або 1,342 кг / м³ (н. У.), Ρжідк. = 0,561 г / см³ (T = -100 ° C). Тиск парів при 0 ° C - 2,379 МПа. Розчинність в воді - 4,7 мл в 100 мл (при 20 ° C), в етанолі - 46 мл в 100 мл (при 0 ° C), добре розчиняється в вуглеводнях . точка спалаху у етану дорівнює -187,8 ° C, температура самозаймання - 595 ° C. Етан утворює з повітрям вибухонебезпечні суміші при вмісті 5-15 об. % (При 20 ° C). Октанове число -120,3 [2] [3] [4] .
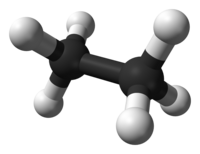
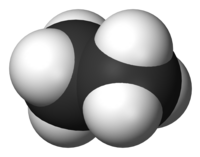
Молекула етану має тетраедричну будову: атоми вуглецю є sp3- гібридними . Зв'язок C-C утворена перекриванням sp3-гібридних орбіталей , А зв'язок C-H - перекриванням sp3-гібридної орбіталі вуглецю і s-орбіталі водню . Довжина зв'язку C-C дорівнює 1,54 Å, а довжина зв'язку C-H дорівнює 1,095 Å [5] .
Оскільки С-С-зв'язок в етан одинарна, навколо неї можливо вільне обертання метильних груп. При обертанні виникають різні просторові форми молекули етану, які називаються конформаціями . Конформації прийнято зображати у вигляді перспективного зображення (такі зображення іноді називають «лісопильними козлами») або у вигляді проекцій Ньюмена [5] .
Число конформаций для етану нескінченно, однак прийнято розглядати дві крайні конформації:
- заслоненних, в якій атоми водню максимально зближені в просторі;
- і загальмовану, в якій атоми водню максимально віддалені [5] .
Затулена конформація має найбільшу енергію з усіх конформаций, а загальмована - найменшу, тобто є найбільш енергетично вигідною і, отже, більш стійкою. Різниця енергії між цими конформаціями дорівнює 2,9 ккал / моль. Вважається, що це число відображає торсіонне напруга в менш вигідною заслоненних конформації. Якщо розділити цю енергію на три взаємодії між парами атомів водню, то енергія торсіонного взаємодії двох атомів водню складе приблизно 1 ккал / моль [5] .
За значенням 2,9 ккал / моль з рівняння Гіббса можна обчислити константу рівноваги між двома конформаціями етану. При температурі 25 ° С значно переважає загальмована конформація: 99% молекул етану знаходяться в цій конформації і лише 1% - в заслоненних [5] .
Енергії крайніх і проміжних конформацій прийнято представляти у вигляді циклічних графіків, де по осі абсцис відкладений торсіонний кут, а по осі ординат - енергія.
У промисловості [ правити | правити код ]
У промисловості отримують з нафтових і природних газів , Де він становить до 10% за обсягом. У Росії зміст етану в нафтових газах дуже низька. В США і Канаді (Де його зміст в нафтових і природних газах високо) служить основною сировиною для отримання етилену [6] . Також етан отримують при гідрокрекінгу вуглеводнів і зрідження вугілля [7] .
У лабораторних умовах [ правити | правити код ]
У 1848 році Кольбе і Франкленд вперше синтетично отримали етан, обробивши пропіонітрил металевим калієм . У 1849 році вони отримали цей газ електролізом ацетату калію і дією цинку і води на йодоетан [8] .
У лабораторії етан можна отримати декількома способами:
2 C H 3 I + 2 N a → C H 3 C H 3 + 2 N a I {\ displaystyle {\ mathsf {2CH_ {3} I + 2Na \ rightarrow CH_ {3} CH_ {3} + 2NaI}}} CH 3 COO - - e - → CH 3 COO ⋅ → CH 3 ⋅ + CO 2 {\ displaystyle {\ mathsf {CH_ {3} COO ^ {-} - e ^ {-} \ rightarrow CH_ {3} COO \ cdot \ rightarrow CH_ {3} \ cdot + CO_ {2}}}}
2 C H 3 ⋅ → C H 3 C H 3 {\ displaystyle {\ mathsf {2CH_ {3} \ cdot \ rightarrow CH_ {3} CH_ {3}}}}
CH 3 CH 2 COON a + N a OH → CH 3 CH 3 + N a 2 CO 3 {\ displaystyle {\ mathsf {CH_ {3} CH_ {2} COONa + NaOH \ rightarrow CH_ {3} CH_ {3} + Na_ {2} CO_ {3}}}}
C H 3 C H 2 B r + M g → C H 3 C H 2 M g B r {\ displaystyle {\ mathsf {CH_ {3} CH_ {2} Br + Mg \ rightarrow CH_ {3} CH_ {2} MgBr}}}
CH 3 CH 2 M g B r + H 2 O → CH 3 CH 3 + M g OHB r {\ displaystyle {\ mathsf {CH_ {3} CH_ {2} MgBr + H_ {2} O \ rightarrow CH_ {3} CH_ {3} + MgOHBr}}}
C H 2 C H 2 + H 2 → C H 3 C H 3 {\ displaystyle {\ mathsf {CH_ {2} CH_ {2} + H_ {2} \ rightarrow CH_ {3} CH_ {3}}}}
H C ≡ C H + 2 H 2 → C H 3 C H 3 {\ displaystyle {\ mathsf {HC \ equiv CH + 2H_ {2} \ rightarrow CH_ {3} CH_ {3}}}}
Етан вступає в типові реакції алканів , Перш за все реакції заміщення, що проходять по свободнорадикальному механізму. Серед хімічних властивості етану можна виділити:
Основне використання етану в промисловості - отримання етилену методом парового крекінгу . Саме з етилену далі отримують важливі промислові продукти, проте в цілях економії розробляються методи перетворення в них самого етану. Однак жоден з проектів поки не пройшов пілотну стадію. Проблеми в цій галузі пов'язані з низькою селективністю реакцій. Одним з перспективних напрямків є синтез вінілхлориду безпосередньо з етану. Також застосовується перетворення етану в оцтову кислоту . Термічним хлоруванням етану в різних умовах отримують хлоретан , 1,1-дихлоретан і 1,1,1-трихлоретан [7] .
Етан має слабку наркотичну дію (ослаблене за рахунок низької розчинності в рідинах організму). клас небезпеки - четвертий [9] . У концентраціях 2-5 об. % Він викликає задишку , В помірних концентраціях - головні болі , сонливість , запаморочення , Підвищене слиновиділення, блювоту і втрату свідомості через нестачу кисню . У високих концентраціях етан може викликати серцеву аритмію , зупинку серця і зупинку дихання . При постійному контакті може виникнути дерматит . Повідомляється, що при 15-19 об. % Етан викликає підвищення чутливості міокарда до катехоламінів [10] .
Імовірно, на поверхні титана (Супутник Сатурна) в умовах низьких температур (-180 ° C) існують цілі озера і річки з рідкої метано-метанова суміші [11] .
- ↑ Ethane (неопр.). Sigma-Aldrich. Дата обігу 6 квітня 2019.
- ↑ Ullmann, 2014 , P. 3-5.
- ↑ 1 2 3 Хімічна енциклопедія .
- ↑ Рабинович В. А., Хавін З. Я. Короткий хімічний довідник. - Изд. 2-е. - Хімія, 1978. - С. 199.
- ↑ 1 2 3 4 5 Реутов О. А., Курц А. Л., Бутін К. П. Органічна хімія: у 4 т.. - 5-е изд. - БИНОМ. Лабораторія знань, 2014. - Т. 1. - С. 321-326. - ISBN 978-5-9963-1535-2 .
- ↑ Хімічна енциклопедія, 1998. .
- ↑ 1 2 Ullmann, 2014 , P. 13.
- ↑ Інтерес .
- ↑ Газохроматографическое вимір масових концентрацій вуглеводнів: метану, етану, етилену, пропану, пропілену, нбутана, альфа-бутилену, изопентана в повітрі робочої зони. Методичні вказівки. МУК 4.1.1306-03
- ↑ Ullmann, 2014 , P. 61.
- ↑ Mousis O., Schmitt B. (квітень 2008). "Sequestration of Ethane in the Cryovolcanic Subsurface of Titan" . The Astrophysical Journal. 677. DOI : 10.1086 / 587141 .
- Братков А. А. Етан // Хімічна енциклопедія: у 5 т / Зефиров Н. С. (гол. Ред.) . - М.: Велика Російська енциклопедія , 1998. - Т. 5: Триптофан-Ятрохімія. - С. 491. - 783 с. - 10 000 прим. - ISBN 5-85270-310-9 .
- Schmidt R., Griesbaum K., Behr A., Biedenkapp D., Voges H.-W., Garbe D., Paetz C., Collin G., Mayer D., Höke H. Hydrocarbons (англ.) // Ullmann's Encyclopedia of Industrial Chemistry. - Wiley, 2014. - DOI : 10.1002 / 14356007.a13_227.pub3 .
- The chemistry of alkanes and cycloalkanes / Ed. Saul Patai and Zvi Rappoport. - John Wiley & Sons, 1992. - ISBN 0-471-92498-9 .
- Тутурін Н. Н. Етан // Енциклопедичний словник Брокгауза і Ефрона : В 86 т. (82 т. І 4 доп.). - СПб. , 1890-1907.